肿瘤坏死因子(TNF)是少数可以进行靶向治疗炎症性疾病的细胞因子之一。然而,靶向TNF的靶向治疗可能会引起显著的副作用。更系统性地认识TNF功能及信号通路将为开发更有针对性的治疗提供基础。
蛋白组学领军人物之一Matthias Mann教授团队利用DIA磷酸化蛋白质组学技术解析了TNF介导的大量磷酸化事件,并利用DIA蛋白质组学和DIA磷酸化蛋白质组学揭示了CDK在TNF信号通路中的重要作用。研究成果以“Phosphoproteome profiling uncovers a key role for CDKs in TNF signaling”为题,发表在Nature Communications(中科院JCR一区,IF:14.919 )上。
研究过程
在TNF刺激的5min内,参与囊泡融合和髓系细胞分化调控的蛋白的磷酸化状态增加,而涉及RIG-I、NF-κB、TRIF和MYD88通路以及GTPase激活的条目则出现在15min之后。与转录相关的条目在整个时间过程中都受到调控,且在最近的时间点最为强烈,这与转录是TNF信号级联的最下游过程相一致。Motif富集分析显示了不同激酶沿时间过程的动态激活。CDK1/2和PLK1/3的磷酸化motif表达下调,而IKBKB(IKK2)和PRKAA1/2磷酸化motif在早期时间点表达上调。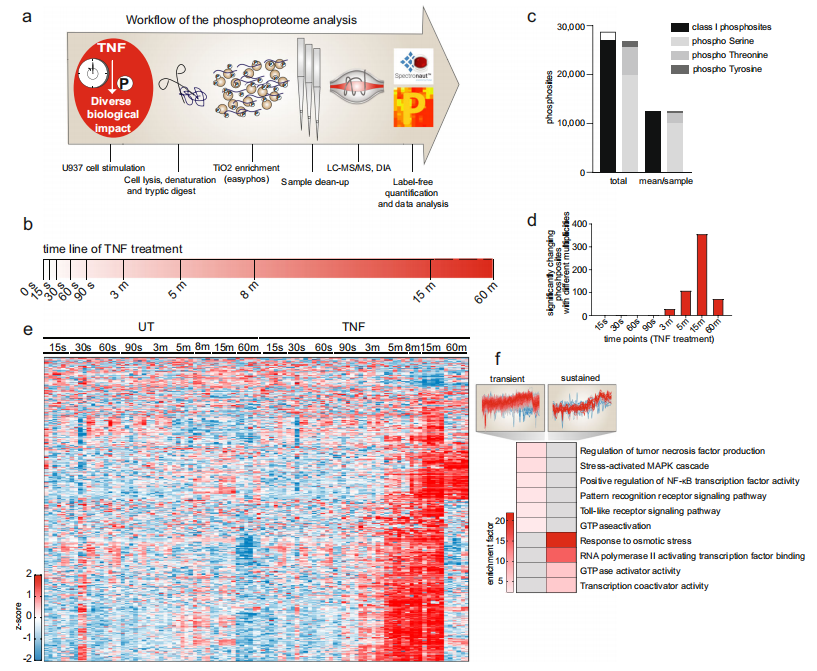
研究者同时对其他细胞系在TNF处理15min后的磷酸化事件进行检测,这些细胞系包括A549(腺癌肺泡基底上皮细胞系)、HT29(结直肠腺癌细胞系)和U2OS(骨肉瘤细胞系)和小鼠骨髓源性巨噬细胞(BMDMs)。许多在TNF处理下显著调控的磷酸化事件在不同的人类细胞系中是共享的。
相比之下,抑制下游激酶如IKK1/2、p38、MEK1/2和JNK对TNF调控的磷酸化位点有些微到中等的影响。抑制p38的影响最强,降低了76%的TNF 上调的磷酸化位点。在STRING蛋白相互作用网络中,TNF刺激下与其他磷酸化蛋白不相关的蛋白可以被划为上游激酶。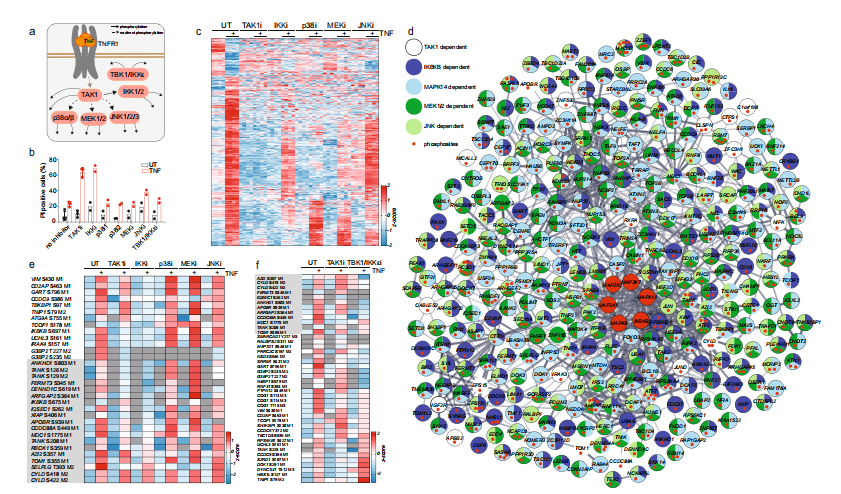
![]()
研究者从有无TAK1抑制剂的TNF处理15min的细胞中分离细胞膜、细胞核和细胞质,并进行了这些亚细胞组分的DIA蛋白质组学和DIA磷酸化蛋白质组检测(未处理组、TNF处理和TNF+TAK1i处理组,各3种亚细胞组分,共9组,生物学重复均为n=4)。
在TNF刺激下,NF-κB必需调节因子(NEMO或IKBKG)、TRAF2和TNIP1水平在细胞膜中升高。其他一些蛋白质也易位到细胞膜部分。一些蛋白质在TNF处理后从细胞膜中脱离出来。在TNF刺激的15min内,触发了许多参与转录的蛋白的核易位,表明存在转录反应。大多数激酶,包括TAK1(MAP3K7)、p38(MAPK14)、IKK2(IKBKB)和MEK1/2(MAP2K1/2),主要富集于细胞质中,而不依赖于TNF的刺激。然而,TNF调控的这些激酶下游蛋白上的磷酸化位点在所有的细胞亚组分中都有富集。其中大部分依赖于定位在细胞质中的TAK1的活性,这意味着TNF触发了激酶及其底物的蛋白易位。研究者甚至检测到了蛋白质组学中未检测到的肽段上的TNF调控的磷酸化事件。这表明这些底物的磷酸化作用触发了易位,或者在易位时,蛋白质立即被磷酸化。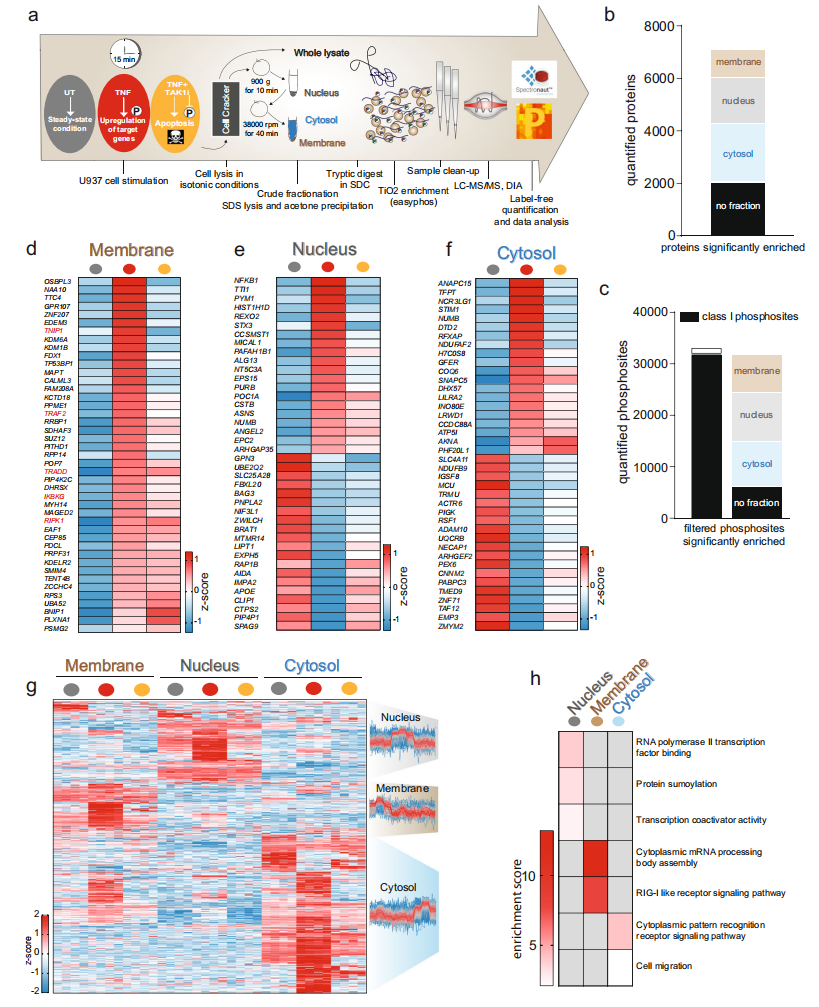
通过靶向TAK1和IKK2来抑制NF-κB信号通路,可诱导TNF下游的细胞死亡。这种细胞死亡可以是凋亡也可以是坏死。为了探索磷酸化事件调节细胞死亡的作用,研究者用TNF处理3h或与cIAP抑制剂 Smac mimetic(SM)联用诱导U937细胞凋亡,或与Smac mimetic(SM)和caspase抑制剂Idun(IDN-6556)诱导细胞坏死,并进行DIA蛋白质组学和DIA磷酸化蛋白质组学检测(未处理组、TNF处理组、TNF+SM组和TM+SM+IDN-6556组,共4组,每组生物学重复均为n=4)。研究者还在BMDM细胞中进行了实验。研究者发现细胞凋亡过程中,两种细胞类型中参与RNA剪接和mRNA加工的蛋白质上的磷酸位点显著上调(U937细胞中344个磷酸位点,BMDMs中123个磷酸位点)。刺激诱导的磷酸化蛋白质组变化与蛋白质组的变化无关。磷酸化的激酶富集分析显示了细胞凋亡过程中周期蛋白依赖性蛋白激酶(CDK)的调控。对刺激后CDKs上显著变化的磷酸位点进行分析,发现是转录性的CDKs(CDK7、9、12、13和14)受到调控,而不是参与了细胞周期调控的CDKs。后续实验表明TNF信号通路诱导细胞磷酸化,从而诱导CDK9和CDK12/13介导的RPB1的激活。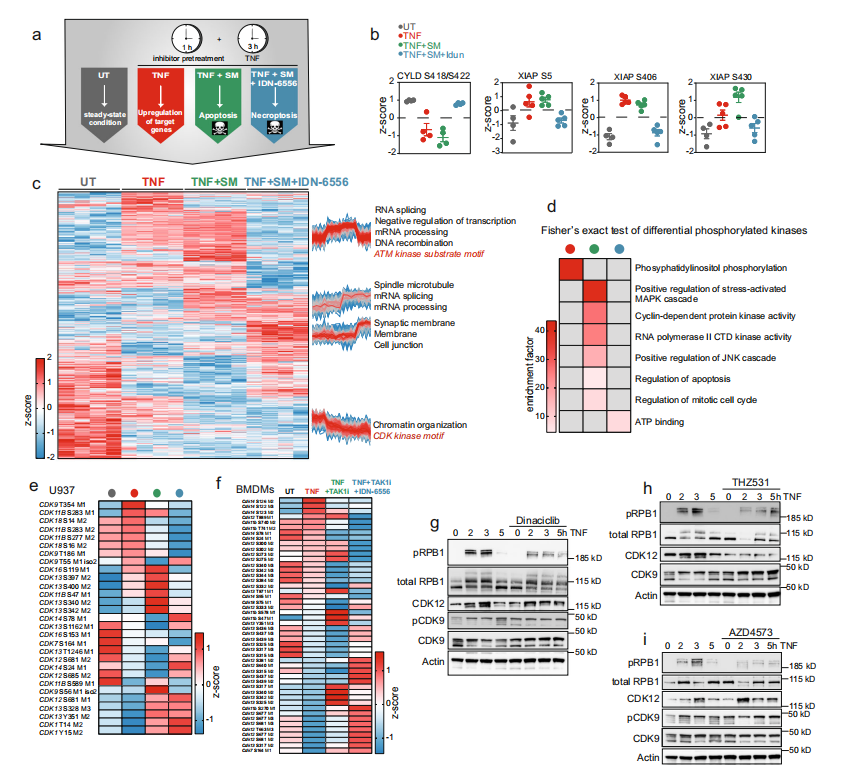
![]()
TNF通过诱导广泛的靶基因触发强大的转录反应。其促炎特性主要是通过上调细胞因子来调节免疫反应,而促存活基因的上调则可以防止细胞过度死亡和炎症。研究者的数据表明,RPB1磷酸化受到调控,由于该蛋白是TNF介导的转录所必需的,研究者想知道抑制转录性的CDKs是否会影响TNF诱导的靶基因表达。
CDK抑制剂处理的细胞的磷酸化蛋白质组学(TNF处理与否(共2组)和TNF±各CDK抑制剂组(共6组),共8组,每组生物学重复n=4)显示,TNF诱导的CDK12/13磷酸化以及早期和晚期的RNA加工受到抑制。有趣的是,对TNF处理的U937细胞的蛋白质组学分析显示,Dinaciclib(CDK1/2/5抑制剂)或两种CDK12抑制剂CDK12-in345和THZ531几乎完全消除了蛋白调控。这些CDK抑制剂也不同程度降低了经典靶基因ICAM1和SOD2的上调。CDK抑制消除了XIAP的轻微下调,这表明这种调控依赖于转录。NF-κB信号通路作为驱动TNF诱导转录的主要途径则不受影响。为了验证CDK抑制剂确实在转录水平上抑制了靶基因的表达,研究者检测了它们对TNF介导的CCL2(MCP1)和CXCL10(IP10)mRNA水平上调的影响,这些基因的mRNA水平确实降低了。同样,加入CDK抑制剂后,小鼠骨髓源性巨噬细胞(BMDMs)释放的细胞因子IP10较少。这与之前研究CDK9作用的研究一致,这表明抑制转录性的CDKs9、12和13可能在疾病中具有抗炎作用。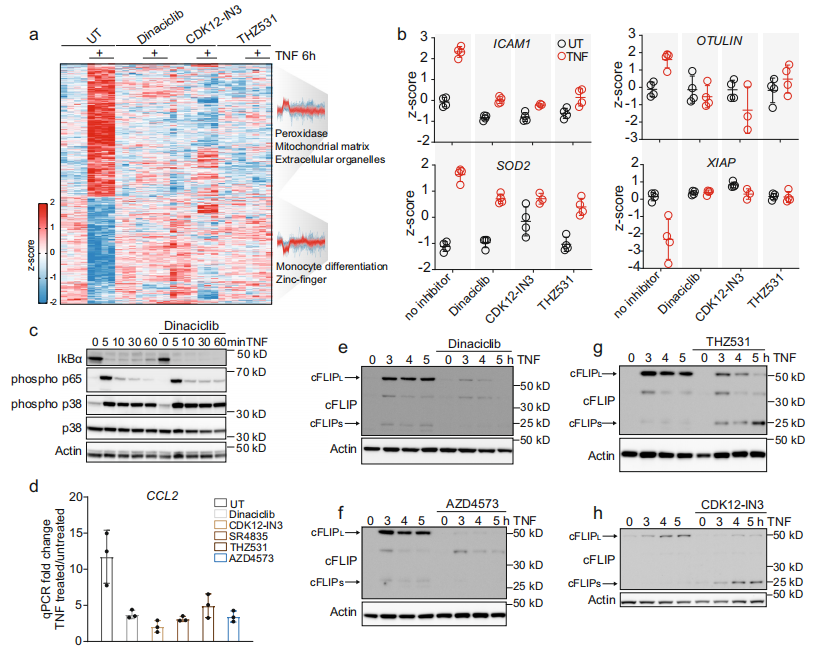
研究者进一步想知道通过转录性CDK抑制剂抑制TNF介导的FLIP上调是否会增强TNF诱导的细胞死亡。用泛CDK抑制剂或其他不同CDK抑制剂处理细胞,均与TNF、TNF +Smac mimetic (SM)或SM +IDN-6556联合一样触发协同细胞死亡。靶向不参与转录的CDKs的抑制剂未能诱导协同细胞死亡。这些实验表明,转录性的,而不是非转录性的CDKs加剧了TNF诱导的细胞死亡。
为了检测CDK抑制剂是否也增强了TNF依赖的坏死,研究者使用SM和caspase 抑制剂IDN-655652联合处理U937细胞。在野生型U937细胞中,CDK抑制也增强了CDK12/13的坏死,而缺乏坏死介导因子MLKL和RIPK3的细胞未能死亡。协同诱导细胞凋亡并不局限于U937细胞,也存在于A549细胞、HT29细胞、U2OS细胞、小鼠皮肤成纤维细胞(MDFs)和小鼠BMDMs中。仅使用TNF并不足以诱导这些细胞的协同死亡,这表明抑制CDK只能增强而不能触发细胞死亡。研究者的结论是,TNF介导的转录性的CDKs调控导致其底物的磷酸化和调控,包括RPB1的CTD。这个最大的RNA聚合酶II亚基对于FLIP等促存活蛋白的转录是必需的,其磷酸化对于防止细胞凋亡和坏死是必要的。不同细胞系中的细胞死亡数据表明,CDK抑制剂加重细胞死亡取决于它们对TNF介导的细胞凋亡和坏死的敏感性。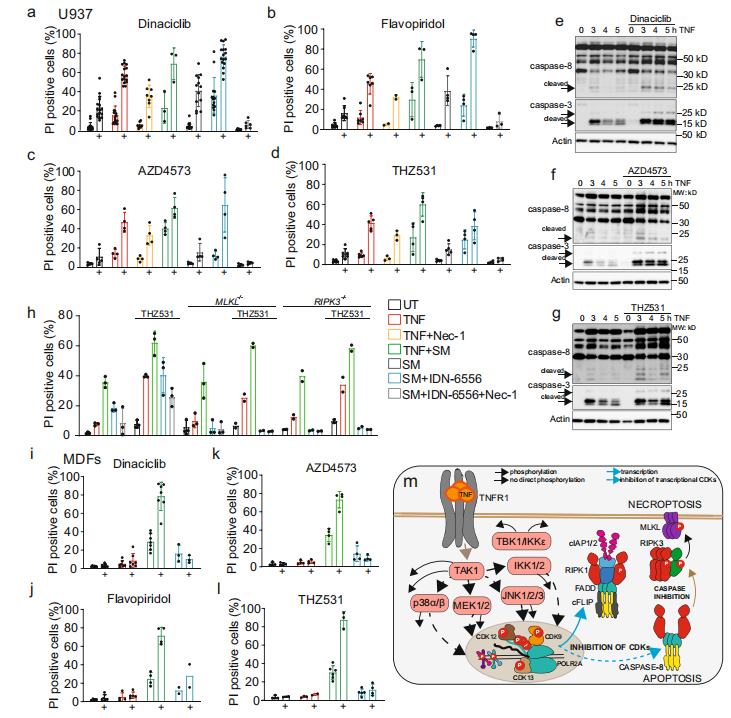
研究总结
本研究通过DIA磷酸化蛋白质组学深入分析了TNF刺激不同时间后诱导的下游磷酸化信号事件。通过亚细胞组分的DIA蛋白质组学和DIA磷酸化蛋白质组学揭示了磷酸化依赖性的蛋白质易位。对TNF诱导凋亡和坏死细胞的DIA磷酸化蛋白质组分析揭示了转录周期蛋白依赖性激酶(CDK)活性在促进细胞因子产生和防止TNF信号受体下游的细胞过度死亡方面的关键作用。
吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和高通量测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组、Olink蛋白质组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·高通量测序平台分为常规测序服务和单细胞测序服务:单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞TCR/BCR、单细胞(RNA+ATAC)、空间转录组测序等服务;常规测序服务提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修饰测序)、acRIP-seq(ac4C RNA乙酰化修饰测序)、ATAC-seq、Ribo-seq(翻译组测序) 、mRNA/miRNA/LncRNA/circRNA-seq、全转录组测序(两文库/三文库)、外泌体miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服务。

研究过程
1. DIA磷酸化蛋白质组学揭示TNF处理不同时间诱导的磷酸化事件
为了系统性揭示TNF下游磷酸化事件及动力学图景,研究者用TNF处理髓系细胞系U937,时间为15秒到1小时(处理组和非处理组各10个时间梯度,共20组,生物学重复n=6),并进行DIA 磷酸化蛋白组学检测。共检测到超过60000个磷酸化肽段,其中28000个肽段有高重复性(高可信)。TNF诱导的磷酸位点在15min达到峰值,但在处理3min后检测到显著的上调,且在60min时恢复到基线水平。许多这些瞬时磷酸化修饰蛋白参与了NF-κB和模式识别信号传导,一小簇转录相关蛋白的磷酸化位点在TNF刺激后60min仍然保持上调。在TNF刺激的5min内,参与囊泡融合和髓系细胞分化调控的蛋白的磷酸化状态增加,而涉及RIG-I、NF-κB、TRIF和MYD88通路以及GTPase激活的条目则出现在15min之后。与转录相关的条目在整个时间过程中都受到调控,且在最近的时间点最为强烈,这与转录是TNF信号级联的最下游过程相一致。Motif富集分析显示了不同激酶沿时间过程的动态激活。CDK1/2和PLK1/3的磷酸化motif表达下调,而IKBKB(IKK2)和PRKAA1/2磷酸化motif在早期时间点表达上调。

研究者同时对其他细胞系在TNF处理15min后的磷酸化事件进行检测,这些细胞系包括A549(腺癌肺泡基底上皮细胞系)、HT29(结直肠腺癌细胞系)和U2OS(骨肉瘤细胞系)和小鼠骨髓源性巨噬细胞(BMDMs)。许多在TNF处理下显著调控的磷酸化事件在不同的人类细胞系中是共享的。
2. 抑制激酶揭示了TNF刺激下激酶-底物的关系
由于在TNF刺激下许多下游激酶的同时激活,对特定的激酶-底物关系的识别仍然具有挑战性。为了解决这个问题,研究者使用特定的抑制剂靶向关键激酶对细胞进行处理,并进行DIA磷酸化蛋白组学检测(TNF处理与否(2组)和激酶抑制剂±TNF处理(10组),共12组,生物学重复n=4)。虽然单独TNF就诱导了数百个磷酸化事件的调控,但抑制TAK1几乎完全消除了这种作用。这证实了TAK1在TNF信号通路上游的作用。相比之下,抑制下游激酶如IKK1/2、p38、MEK1/2和JNK对TNF调控的磷酸化位点有些微到中等的影响。抑制p38的影响最强,降低了76%的TNF 上调的磷酸化位点。在STRING蛋白相互作用网络中,TNF刺激下与其他磷酸化蛋白不相关的蛋白可以被划为上游激酶。

3. 亚细胞组分的DIA蛋白组学和DIA磷酸化蛋白组学揭示TNF介导的磷酸化诱导了广泛的蛋白质易位
研究者从有无TAK1抑制剂的TNF处理15min的细胞中分离细胞膜、细胞核和细胞质,并进行了这些亚细胞组分的DIA蛋白质组学和DIA磷酸化蛋白质组检测(未处理组、TNF处理和TNF+TAK1i处理组,各3种亚细胞组分,共9组,生物学重复均为n=4)。
在TNF刺激下,NF-κB必需调节因子(NEMO或IKBKG)、TRAF2和TNIP1水平在细胞膜中升高。其他一些蛋白质也易位到细胞膜部分。一些蛋白质在TNF处理后从细胞膜中脱离出来。在TNF刺激的15min内,触发了许多参与转录的蛋白的核易位,表明存在转录反应。大多数激酶,包括TAK1(MAP3K7)、p38(MAPK14)、IKK2(IKBKB)和MEK1/2(MAP2K1/2),主要富集于细胞质中,而不依赖于TNF的刺激。然而,TNF调控的这些激酶下游蛋白上的磷酸化位点在所有的细胞亚组分中都有富集。其中大部分依赖于定位在细胞质中的TAK1的活性,这意味着TNF触发了激酶及其底物的蛋白易位。研究者甚至检测到了蛋白质组学中未检测到的肽段上的TNF调控的磷酸化事件。这表明这些底物的磷酸化作用触发了易位,或者在易位时,蛋白质立即被磷酸化。

4. TNF诱导的细胞死亡触发了强烈的RNA加工反应和CDK激活
通过靶向TAK1和IKK2来抑制NF-κB信号通路,可诱导TNF下游的细胞死亡。这种细胞死亡可以是凋亡也可以是坏死。为了探索磷酸化事件调节细胞死亡的作用,研究者用TNF处理3h或与cIAP抑制剂 Smac mimetic(SM)联用诱导U937细胞凋亡,或与Smac mimetic(SM)和caspase抑制剂Idun(IDN-6556)诱导细胞坏死,并进行DIA蛋白质组学和DIA磷酸化蛋白质组学检测(未处理组、TNF处理组、TNF+SM组和TM+SM+IDN-6556组,共4组,每组生物学重复均为n=4)。研究者还在BMDM细胞中进行了实验。研究者发现细胞凋亡过程中,两种细胞类型中参与RNA剪接和mRNA加工的蛋白质上的磷酸位点显著上调(U937细胞中344个磷酸位点,BMDMs中123个磷酸位点)。刺激诱导的磷酸化蛋白质组变化与蛋白质组的变化无关。磷酸化的激酶富集分析显示了细胞凋亡过程中周期蛋白依赖性蛋白激酶(CDK)的调控。对刺激后CDKs上显著变化的磷酸位点进行分析,发现是转录性的CDKs(CDK7、9、12、13和14)受到调控,而不是参与了细胞周期调控的CDKs。后续实验表明TNF信号通路诱导细胞磷酸化,从而诱导CDK9和CDK12/13介导的RPB1的激活。

5. CDK激酶的活性是TNF靶基因转录所必需的
TNF通过诱导广泛的靶基因触发强大的转录反应。其促炎特性主要是通过上调细胞因子来调节免疫反应,而促存活基因的上调则可以防止细胞过度死亡和炎症。研究者的数据表明,RPB1磷酸化受到调控,由于该蛋白是TNF介导的转录所必需的,研究者想知道抑制转录性的CDKs是否会影响TNF诱导的靶基因表达。
CDK抑制剂处理的细胞的磷酸化蛋白质组学(TNF处理与否(共2组)和TNF±各CDK抑制剂组(共6组),共8组,每组生物学重复n=4)显示,TNF诱导的CDK12/13磷酸化以及早期和晚期的RNA加工受到抑制。有趣的是,对TNF处理的U937细胞的蛋白质组学分析显示,Dinaciclib(CDK1/2/5抑制剂)或两种CDK12抑制剂CDK12-in345和THZ531几乎完全消除了蛋白调控。这些CDK抑制剂也不同程度降低了经典靶基因ICAM1和SOD2的上调。CDK抑制消除了XIAP的轻微下调,这表明这种调控依赖于转录。NF-κB信号通路作为驱动TNF诱导转录的主要途径则不受影响。为了验证CDK抑制剂确实在转录水平上抑制了靶基因的表达,研究者检测了它们对TNF介导的CCL2(MCP1)和CXCL10(IP10)mRNA水平上调的影响,这些基因的mRNA水平确实降低了。同样,加入CDK抑制剂后,小鼠骨髓源性巨噬细胞(BMDMs)释放的细胞因子IP10较少。这与之前研究CDK9作用的研究一致,这表明抑制转录性的CDKs9、12和13可能在疾病中具有抗炎作用。

6. 转录性CDKs可抑制TNF诱导的细胞死亡
研究者进一步想知道通过转录性CDK抑制剂抑制TNF介导的FLIP上调是否会增强TNF诱导的细胞死亡。用泛CDK抑制剂或其他不同CDK抑制剂处理细胞,均与TNF、TNF +Smac mimetic (SM)或SM +IDN-6556联合一样触发协同细胞死亡。靶向不参与转录的CDKs的抑制剂未能诱导协同细胞死亡。这些实验表明,转录性的,而不是非转录性的CDKs加剧了TNF诱导的细胞死亡。
为了检测CDK抑制剂是否也增强了TNF依赖的坏死,研究者使用SM和caspase 抑制剂IDN-655652联合处理U937细胞。在野生型U937细胞中,CDK抑制也增强了CDK12/13的坏死,而缺乏坏死介导因子MLKL和RIPK3的细胞未能死亡。协同诱导细胞凋亡并不局限于U937细胞,也存在于A549细胞、HT29细胞、U2OS细胞、小鼠皮肤成纤维细胞(MDFs)和小鼠BMDMs中。仅使用TNF并不足以诱导这些细胞的协同死亡,这表明抑制CDK只能增强而不能触发细胞死亡。研究者的结论是,TNF介导的转录性的CDKs调控导致其底物的磷酸化和调控,包括RPB1的CTD。这个最大的RNA聚合酶II亚基对于FLIP等促存活蛋白的转录是必需的,其磷酸化对于防止细胞凋亡和坏死是必要的。不同细胞系中的细胞死亡数据表明,CDK抑制剂加重细胞死亡取决于它们对TNF介导的细胞凋亡和坏死的敏感性。

研究总结
本研究通过DIA磷酸化蛋白质组学深入分析了TNF刺激不同时间后诱导的下游磷酸化信号事件。通过亚细胞组分的DIA蛋白质组学和DIA磷酸化蛋白质组学揭示了磷酸化依赖性的蛋白质易位。对TNF诱导凋亡和坏死细胞的DIA磷酸化蛋白质组分析揭示了转录周期蛋白依赖性激酶(CDK)活性在促进细胞因子产生和防止TNF信号受体下游的细胞过度死亡方面的关键作用。
吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和高通量测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组、Olink蛋白质组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·高通量测序平台分为常规测序服务和单细胞测序服务:单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞TCR/BCR、单细胞(RNA+ATAC)、空间转录组测序等服务;常规测序服务提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修饰测序)、acRIP-seq(ac4C RNA乙酰化修饰测序)、ATAC-seq、Ribo-seq(翻译组测序) 、mRNA/miRNA/LncRNA/circRNA-seq、全转录组测序(两文库/三文库)、外泌体miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服务。
